Aminozuren vormen de fundamentele bouwstenen van eiwitten, die essentieel zijn voor vrijwel alle biologische processen in levende organismen. De term "alfa-koolstofatoom" is cruciaal voor het begrijpen van de structuur en functie van de meeste aminozuren die in eiwitten voorkomen.
De naamgeving met alfa-, beta- en dergelijke heeft betrekking op de plaatsing van een functionele groep in moleculen met meer dan 1 functionele groep. Het "alfa" atoom is het eerste atoom naast het C-atoom met de ene functionele groep, het beta-atoom de tweede en dergelijke. Het wordt vaak toegepast als de ene functionele groep tot gevolg heeft dat er een quaternair C-atoom ontstaat, bijvoorbeeld bij zuren en esters. In het geval van aminozuren kan de aminegroep dus op het eerste C-atoom naast de zuurgroep zitten, dan is het een alfa-aminozuur zoals men die voornamelijk kent in de biochemie. Zit de aminegroep één C-atoom verder, dan wordt het dus een beta-aminozuur. Nemen we als voorbeeld alanine, dan is (alfa)-alanine 2-aminopropaanzuur. Plaats je de aminogroep eentje verderop, dan wordt het 3-aminopropaanzuur en noemen we het beta-alanine. Men tekent alfa-alanine vaak met de CH3-groep alszijnde een substituent van een 2-aminoethaanzuur "backbone", maar voor de werkelijke structuur maakt het niet uit hoe je het tekent. Dezelfde truc kun je voor bijna alle andere aminozuren toepassen.
Wat zijn Aminozuren?
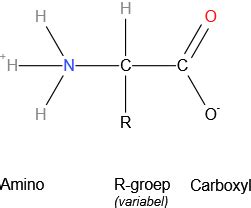
Een aminozuur is een organische verbinding die zowel een carboxygroep (-COOH) als een aminegroep (-NH2) bezit. Meestal worden in de biochemie met aminozuren specifiek α-aminozuren bedoeld. Bij dit soort verbindingen staan de carboxygroep en de aminogroep op hetzelfde (meestal chirale) koolstofatoom. α-aminozuren, ook wel, maar niet correct, proteïnogene aminozuren genoemd, zijn de bouwstenen van peptiden, polypeptiden en eiwitten. De algemene formule voor een α-aminozuur is R-CH(NH2)-COOH. De R staat voor Residu-groep, een functionele groep die er op deze plaats aan vast kan zitten.
Aminozuren zijn een groep organische verbindingen waarvan de structuur bestaat uit de atomen koolstof, stikstof, waterstof en zuurstof, evenals een variabele laterale ketengroep. Hun naam is een verkorte vorm van de term “α-aminocarbonzuur”. Als we het hebben over verschillende soorten aminozuren, vervangen we vaak hun systematische namen door gebruikelijke namen. De belangrijkste indeling van aminozuren is in eiwit- en niet-eiwittypen. De eerste groep omvat ongeveer twintig verbindingen, die elk een onderdeel zijn van eiwitten en cruciaal zijn voor het menselijk lichaam. Deze eiwitten, die ook als structurele moleculen in planten en dieren voorkomen, spelen een fundamentele rol door deel te nemen aan veel mechanismen die verantwoordelijk zijn voor het handhaven van de homeostase in het menselijk lichaam.
Essentiële en Niet-Essentiële Aminozuren
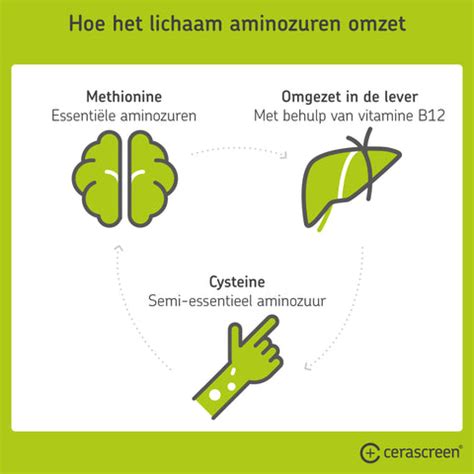
Tijdens de spijsvertering worden aminozuren, onder invloed van enzymen, uit in de voeding aanwezige eiwitten vrijgemaakt (hydrolyse). Uit de vrijgekomen aminozuren kan het organisme zijn eigen specifieke eiwitten weer opbouwen. Het organisme kan een aantal fundamentele aminozuren zelf synthetiseren, andere echter niet. Deze laatste moeten in het voedsel aanwezig zijn, men noemt ze de noodzakelijke of essentiële aminozuren. Exogene aminozuren zijn organische verbindingen die nodig zijn om de homeostase in ons lichaam te behouden, maar ze zijn niet in staat tot zelfproductie. Daarom moeten ze worden verstrekt in de vorm van een passend dieet, samen met goed uitgebalanceerde maaltijden en in de vorm van adequate supplementen. De andere categorie omvat endogene aminozuren, die regelmatig in het menselijk lichaam worden gesynthetiseerd, zodat de vraag ernaar voortdurend op autonome basis wordt gedekt. Dit zijn verbindingen die in het lichaam kunnen worden geproduceerd, maar alleen als er toegang is tot de juiste hoeveelheden van hun voorlopers.
Mensen die lijden aan fenylketonurie kunnen geen fenylalanine afbreken en omzetten in tyrosine en moeten dit dus met het voedsel binnen krijgen. Doordat het fenylalanine zich in het bloed en het ruggenmerg ophoopt, kunnen er zenuwcellen beschadigd raken en treedt uiteindelijk hersenbeschadiging op. Daarom wordt er bij pasgeborenen met een hielprik bloed afgenomen en worden zij op deze afwijking gecontroleerd.
Voor de mens zijn een aantal aminozuren essentieel; het zijn aminozuren die de mens niet zelf uit de andere aminozuren kan maken en die via het voedsel moeten worden opgenomen. Aminozuren in een eiwit kunnen op diverse manieren geïdentificeerd worden. Daartoe wordt het eiwit eerst in brokstukken opgesplitst. Dit kan gebeuren door zure hydrolyse van het eiwit in 6 N zoutzuur bij verhoogde temperatuur. Daarna worden de brokstukken van elkaar gescheiden met behulp van hogedrukvloeistofchromatografie (HPLC), gekleurd met ninhydrine-kleuring en gedetecteerd bij 440 (proline) en 570 nm. Deze methode is bekend onder de naam Moore&Stein zure hydrolyse van eiwitten.
Structuur en Eigenschappen van Alfa-Aminozuren
Bij alle biologisch belangrijke aminozuren zit de amino- en de carboxygroep vast aan hetzelfde koolstofatoom, zodat ze allemaal met de algemene formule R-CH(NH2)-COOH voorgesteld kunnen worden. Het gecombineerde molecuul dat dan is ontstaan heet een amide. Dit opent de mogelijkheid om een keten (polymeer) van aminozuren te maken met behulp van herhaalde kop-staartreacties. Zo'n molecule wordt een peptide genoemd, en afhankelijk van het aantal betrokken aminozuren worden ze di-, tri-, tetra-, pentapeptiden etc. genoemd. Eiwitten zijn polypeptiden en vormen een groot deel van de chemische machinerie van de cel.
Alle α-aminozuren (behalve glycine) hebben een asymmetrisch koolstofatoom (chiraal koolstofatoom). Dit betekent dat deze aminozuren in twee vormen (isomeren) kunnen voorkomen, de L-vorm en de D-vorm - deze twee vormen zijn het spiegelbeeld van elkaar (zie optische isomerie). Deze twee isomeren hebben de eigenschap dat zij het polarisatievlak van gepolariseerd licht over een bepaalde hoek kunnen draaien. Voor eiwitten gebruikt worden L-aminozuren. De R,S-nomenclatuur wordt gebruikt voor het beschrijven van de absolute configuratie. De prioriteit van groepen rond het chirale centrum wordt bepaald op basis van atoomnummer: COOH > CHO > CH2OH > CH3 > H.
De oplosbaarheid hangt voornamelijk af van de polariteit van de zijketen (R) van het α-aminozuur af. Hierdoor kan het α-aminozuur in meer of mindere mate hydrofiel dan wel hydrofoob zijn. Dit beïnvloedt zijn interactie met andere structuren, zowel binnen een eiwit zelf, als met andere eiwitten of omliggend weefsel. Oplosbare eiwitten hebben een oppervlak dat rijk is aan polaire aminozuren zoals serine en threonine, terwijl membraaneiwitten aan de buitenkant hydrofobe aminozuren hebben die zich hechten aan een lipidemembraan. Hydrofobe interacties ontstaan tussen hydrofobe aminozuren, de alifatische en de aromatische aminozuren. Hydrofiele en hydrofobe interacties tussen naburige eiwitten hoeven niet af te hangen van de zijketens van de α-aminozuren.
Bij normale omstandigheden (25 °C, atmosferische druk) zijn α-aminozuren in oplossing geladen, tenzij de zuurgraad (pH) gelijk is aan het iso-elektrisch punt. Het iso-elektrisch punt is de pH waarbij de totale lading van de aminozuur deeltjes nul is. Er zijn dan voornamelijk zwitterionen in de oplossing. De reacties tussen de verschillende vormen zijn allemaal evenwichten. Dit betekent dat in het iso-elektrisch punt naast de twee genoemde vormen van het aminozuur ook de positief geladen vorm (aminogroep heeft een H+ opgenomen, COOH nog niet afgestaan) en de negatief geladen vorm (aminogroep nog neutraal, COOH wel al H+ afgestaan) in gelijke aantallen voorkomen.
Aminozuren
Reacties van Aminozuren
Aminozuren kunnen diverse chemische reacties ondergaan, waaronder:
- Verestering: Synthese van esters door reactie tussen een aminozuur en een alcohol.
- Decarboxylering: Verwarming van een aminozuur in aanwezigheid van een barium(II)hydroxide (Ba(OH)2)-oplossing.
- Deaminatie: Reactie waarbij aminozuren met een primaire aminegroep betrokken zijn. De reactie vindt plaats onder invloed van salpeter(III)zuur (HNO2), waarbij het aminozuur oxideert en een waterstofzuur produceert. De aminegroep komt vrij in de vorm van stikstof.
- Ninhydrinereactie: Een gekleurde reactie waarbij een aminozuur reageert met een ninhydrine-oplossing.
- Xanthoproteïnereactie: Een reactie om aromatische aminozuren, zoals fenylalanine, tyrosine of tryptofaan, te detecteren. Bij behandeling met geconcentreerd salpeterzuur (V) zuur (HNO3) kleurt de verbinding geel.
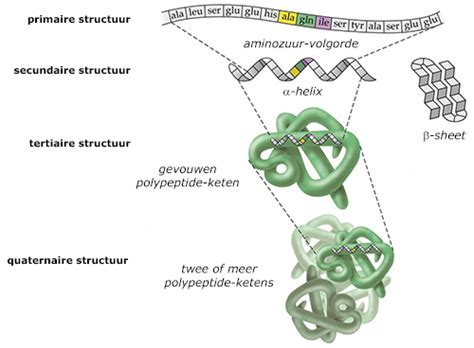
De primaire structuur van een eiwit is de volgorde en de soort van de aminozuren in de keten. De secundaire structuur van een eiwit is de ruimtelijke structuur van een keten met de verbanden binnen de eiwitketen. De tertiaire structuur van een eiwit is de totale ruimtelijke vorm van een eiwitketen. De quaternaire structuur van een eiwit is de totale functiegebonden structuur eventueel in samenhang met meerdere moleculen.
Er zijn twintig α-aminozuren die ten grondslag liggen aan een eiwitstructuur. Circa acht aminozuren zijn essentieel en moeten in de voeding (voor mensen) aanwezig zijn.
Voor het beschrijven van de absolute configuratie van chiraliteit is de R,S-nomenclatuur van belang. De α-koolstofatomen in aminozuren zijn tetraëdraal, behalve voor glycine (waar de zijketen een waterstofatoom is). Dit leidt tot de vorming van D- en L-enantiomeren.
tags: #alfa #koolstofatoom #aminozuur