Aminozuren zijn moleculaire stoffen die als amfolieten fungeren.
Wat zijn Amfolieten?
Amfolieten zijn deeltjes die zowel als zuur als base kunnen reageren. Een voorbeeld van een amfoliet is natriumwaterstofcarbonaat (NaHCO₃). In water splitst het in natriumionen en waterstofcarbonationen. Het waterstofcarbonation kan als zuur reageren door een H+ af te staan, of als base door een H+ op te nemen. Een amfolyt is een deeltje dat zowel als zuur als base kan reageren.
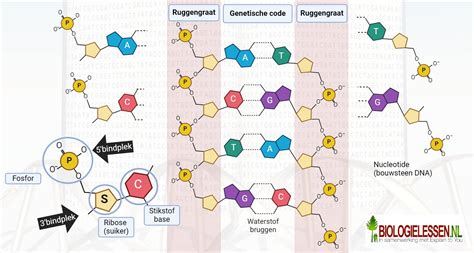
Gedrag in Water
Wanneer natriumwaterstofcarbonaat in water oplost, treden er twee evenwichten op:
- Als zuur: HCO₃⁻ + H₂O ⇌ CO₃²⁻ + H₃O⁺ (Kz = 4,7 x 10⁻¹¹)
- Als base: HCO₃⁻ + H₂O ⇌ H₂CO₃ + OH⁻ (Kb = 2,2 x 10⁻⁸)
De Kz en Kb-waarden bepalen of de oplossing zuur of basisch is. In dit geval is Kb groter dan Kz, wat betekent dat de oplossing basisch is.
Watermoleculen kunnen een proton opnemen (van een zuur) en een proton afgeven (aan een base), waardoor ze amfolyten zijn. De reacties tussen de verschillende vormen zijn allemaal evenwichten. Dit betekent dat in het iso-elektrisch punt naast de twee genoemde vormen van het aminozuur ook de positief geladen vorm (aminogroep heeft een H+ opgenomen, COOH nog niet afgestaan) en de negatief geladen vorm (aminogroep nog neutraal, COOH wel al H+ afgestaan) in gelijke aantallen voorkomen.
Amfolieten in Zure en Basische Oplossingen
Een amfoliet reageert afhankelijk van zijn omgeving:
- In een zure oplossing gedraagt het zich als een base en neemt het een H+ op.
- In een basische oplossing gedraagt het zich als een zuur en staat het een H+ af.
Voorbeeld: H₂PO₄⁻ reageert als base in een zure oplossing en als zuur in een basische oplossing.
Als je een zuur toevoegt zal H₂PO₄⁻ reageren als base. Als je een base toevoegt zal H₂PO₄⁻ reageren als zuur. Beide reacties vinden plaats, alleen evenwicht 1 ligt veel meer rechts dan evenwicht 2. Er wordt dus meer H₃O⁺ gevormd dan OH⁻ en dus zal de oplossing zuur worden en zal H₂PO₄⁻ zich als zuur gedragen.
Kz > Kb? Dan gedraagt een amfolyt zich in water als een zuur. Kb > Kz? Dan gedraagt een amfolyt zich in water als een base.
Aminozuren als Amfolieten
Aminozuren bestaan uit een NH₂-groep en een C=OOH-groep. In water kunnen aminozuren protonen opnemen of afstaan, waardoor ze dubbelionen vormen. De algemene formule voor een α-aminozuur is R-CH(NH₂)-COOH. De R staat voor Residu-groep, een functionele groep die er op deze plaats aan vast kan zitten. Bij alle biologisch belangrijke aminozuren zit de amino- en de carboxygroep vast aan hetzelfde koolstofatoom, zodat ze allemaal met de algemene formule R-CH(NH₂)-COOH voorgesteld kunnen worden.
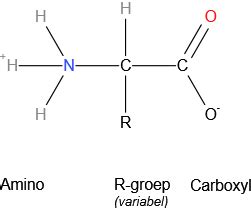
Aminozuren bestaan uit dubbelionen, wat zorgt voor extra aantrekkingskrachten tussen de moleculen. Aminozuren zijn de bouwstenen van peptiden, polypeptiden en eiwitten. Via enzymreacties (protease) in het spijsverteringskanaal worden eiwitten opgesplitst in aminozuren (proteolyse). De aminozuren worden vervolgens door het bloed via de darmhaarvaten en de poortader naar de lever gevoerd. Omdat eiwitsynthese uit aminozuren vooral in de lichaamscellen plaatsvindt, zal een groot deel van de aminozuren de lever onveranderd verlaten. Toch worden ook in de lever (niet-essentiële) aminozuren aangemaakt. Voor de mens zijn een aantal aminozuren essentieel; het zijn aminozuren die de mens niet zelf uit de andere aminozuren kan maken en die via het voedsel moeten worden opgenomen.
Alle α-aminozuren (behalve glycine) hebben een asymmetrisch koolstofatoom (chiraal koolstofatoom). Dit betekent dat deze aminozuren in twee vormen (isomeren) kunnen voorkomen, de L-vorm en de D-vorm - deze twee vormen zijn het spiegelbeeld van elkaar (zie optische isomerie). Deze twee isomeren hebben de eigenschap dat zij het polarisatievlak van gepolariseerd licht over een bepaalde hoek kunnen draaien.
De oplosbaarheid hangt voornamelijk af van de polariteit van de zijketen (R) van het α-aminozuur af. Hierdoor kan het α-aminozuur in meer of mindere mate hydrofiel dan wel hydrofoob zijn. Dit beïnvloedt zijn interactie met andere structuren, zowel binnen een eiwit zelf, als met andere eiwitten of omliggend weefsel. Oplosbare eiwitten hebben een oppervlak dat rijk is aan polaire aminozuren zoals serine en threonine, terwijl membraaneiwitten aan de buitenkant hydrofobe aminozuren hebben die zich hechten aan een lipidemembraan. Hydrofobe interacties ontstaan tussen hydrofobe aminozuren, de alifatische en de aromatische aminozuren. Hydrofiele en hydrofobe interacties tussen naburige eiwitten hoeven niet af te hangen van de zijketens van de α-aminozuren.
Mensen die lijden aan fenylketonurie kunnen geen fenylalanine afbreken en omzetten in tyrosine en moeten dit dus met het voedsel binnen krijgen. Doordat het fenylalanine zich in het bloed en het ruggenmerg ophoopt, kunnen er zenuwcellen beschadigd raken en treedt uiteindelijk hersenbeschadiging op. Daarom wordt er bij pasgeborenen met een hielprik bloed afgenomen en worden zij op deze afwijking gecontroleerd.
Aminozuren
Bij normale omstandigheden (25 °C, atmosferische druk) zijn α-aminozuren in oplossing geladen, tenzij de zuurgraad (pH) gelijk is aan het iso-elektrisch punt.
Proteïnogene aminozuren zijn een subset van α-aminozuren die direct via de genetische code in proteïnes worden ingebouwd. Daarnaast is er nog een aantal aminozuren die na het vertalen van die code gewijzigd worden (bv. cysteïne dat vaak omgezet wordt in cystine). Naast deze twee groepen is er nog een groep aminozuren die niet in proteïnes voorkomt, maar wel een rol speelt in de biochemie (bv.: ornithine) en een heel grote groep die niet uit de biochemie bekend is. Dat laatste betekent dan weer niet dat deze verbindingen biologisch niet actief kunnen zijn.
Hierbij reageert een carboxygroep van het ene molecuul met een amine-groep van een ander molecuul en vormt onder afsplitsing van water (condensatiereactie) een peptidebinding. Het gecombineerde molecuul (ook wel de verbinding genoemd) dat dan is ontstaan heet een amide. Dit opent de mogelijkheid om een keten (polymeer) van aminozuren te maken met behulp van herhaalde kop-staartreacties. Zo'n molecule wordt een peptide genoemd, en afhankelijk van het aantal betrokken aminozuren worden ze di-, tri-, tetra-, pentapeptiden etc. genoemd. Eiwitten zijn polypeptiden en vormen een groot deel van de chemische machinerie van de cel.
In de natuur zijn ongeveer 500 verschillende aminozuren geïdentificeerd, twintig daarvan komen in menselijke eiwitten voor, de zogeheten fundamentele aminozuren. Tijdens de spijsvertering worden aminozuren, onder invloed van enzymen, uit in de voeding aanwezige eiwitten vrijgemaakt (hydrolyse). Uit de vrijgekomen aminozuren kan het organisme zijn eigen specifieke eiwitten weer opbouwen. Het organisme kan een aantal fundamentele aminozuren zelf synthetiseren, andere echter niet. Deze laatste moeten in het voedsel aanwezig zijn, men noemt ze de noodzakelijke of essentiële aminozuren.
Aminoazuren in een eiwit kunnen op diverse manieren geïdentificeerd worden. Daartoe wordt het eiwit eerst in brokstukken opgesplitst. Dit kan gebeuren door zure hydrolyse van het eiwit in 6 N zoutzuur bij verhoogde temperatuur. Daarna worden de brokstukken van elkaar gescheiden met behulp van hogedrukvloeistofchromatografie (HPLC), gekleurd met ninhydrine-kleuring en gedetecteerd bij 440 (proline) en 570 nm. Deze methode is bekend onder de naam Moore&Stein zure hydrolyse van eiwitten.
ω-aminozuren, waarbij de carboxy- en aminogroep aan de uiteinden van (lange) koolstofketens zitten.
Er passen 3,5 aminozuureenheden in een helixwinding. De aanwezigheid van proline zorgt ervoor dat de keten een linksdraaiende spiraal vormt, wat de ruimtelijke structuur beïnvloedt. Cyclische aminozuren zoals proline kunnen niet goed in de helixstructuur van een transmembraandomein worden geïntegreerd.
tags: #dubbelionen #bij #aminozuren