Caseïne is een dierlijk eiwit dat in melk voorkomt en veruit het belangrijkste melkeiwit vormt. Het is verantwoordelijk voor de witte kleur en de hoge voedingswaarde van zuivelproducten en maakt tot 80% uit van het koemelkeiwit, waarbij wei de overige 20% uitmaakt.
Wat is Denaturatie?
Denaturatie van eiwitten, waaronder caseïne, is een proces waarbij de natuurlijke structuur van het eiwit wordt veranderd, wat leidt tot verlies van zijn oorspronkelijke functie. Dit kan gebeuren door verschillende factoren zoals hitte, pH-veranderingen of mechanische bewerking.
Denaturatie van Caseïne door pH-verandering
Als de melkcolloïde verzuurt (lagere pH-waarde), begint de caseïne uit te vlokken, wat resulteert in de klontering van melk. Dit proces, bekend als zure precipitatie, is een vorm van denaturatie. Het meest bekende bereidingsproces voor caseïnaten omvat een zure precipitatie van de caseïne-eiwitten bij een pH van 4,6, gevolgd door het wassen van het neerslag en het opnieuw oplossen van het eiwitcoagulum door pH-verhoging. Bij deze methode, waarbij niet wordt verwarmd, blijven de wei-eiwitten opgelost en worden ze niet mee gewonnen, wat leidt tot een eiwitverlies van ongeveer 20%.
Een belangrijke voordeel dat verkregen wordt door een specifieke werkwijze is dat bij een pH tussen 3 en 4 de caseïne-eiwitten suboptimaal oplosbaar zijn, waardoor de flux door het membraan, zonder dat verstoppingen optreden, relatief hoog kan blijven. Aldus kan, met die hoge flux, een concentratiefaktor van 2,5 worden gehaald. Onder toepassing van de werkwijze volgens de uitvinding wordt een melkeiwit-isolaat verkregen, waarin de caseïne-eiwitten in de vorm van een caseïnaat en de serumeiwitten in natieve vorm aanwezig zijn.
In grafieken 1, 2 en 3 wordt de relatie weergegeven tussen de flux over het membraan en de drukval per trap tijdens de ultrafiltratie van aangezuurde magere melk, bij verschillende pH's. De experimenten werden uitgevoerd met een tweetraps Abcor-systeem. De verschillende flux-waarden hebben betrekking op een continuproces, waarbij magere melk bij een pH van 3, 3,5 en 4 werd geultrafiltreerd. De flux van zowel de eerste als de tweede trap wordt in de grafieken weergegeven bij een concentratiefaktor respectievelijk volumereductie van 2,5 respectievelijk 60%. Uit de gegevens blijkt, dat de gemiddelde flux gedurende een duurproef van 6 uur bij een pH 3 minstens 10% hoger ligt dan bij zowel een pK van 3,5 als een pH van 4,0. In grafiek 4 wordt de invloed van de pH op de capaciteit bij een batchgewijze proces vergeleken.
De viscositeit wordt hoger naarmate de pH wordt verlaagd en ten gevolge van deze viscositeitstoename zal de capaciteit van het ultra-filtratieproces afnemen. Ook de oplosbaarheid neemt toe naarmate de pH verder van het isoelektrische punt zal afliggen, ten gevolge waarvan eveneens de capaciteit, welke immers omgekeerd gerelateerd is aan de oplosbaarheid van het eiwit, zal afnemen.
De pH van de gethemiseerde melk werd bij een temperatuur van 5°C op een waarde van 3 ingesteld, onder toepassing van 4N-zoutzuur. Vervolgens werd de temperatuur batch-gewijze verhoogd naar 50°C, waarna met de genoemde ultrafiltratie-inrichting de melk tot een concentratiefaktor 2,5 werd geconcentreerd.
Denaturatie van Caseïne door Hitte
Een andere belangrijke parameter bij de werkwijze volgens de uitvinding is de temperatuur waarbij de ultrafiltratie wordt toegepast. Voor de meeste membranen geldt een maximaal toelaatbare temperatuur, welke tussen 50 en 60°C ligt. Verder is gebleken, dat in verband met de capaciteit van de werkwijze volgens de uitvinding de verlaging van de pH naar een waarde beneden het isoelektrische punt van caseïne-eiwitten bij voorkeur uitgevoerd moet worden bij lage temperaturen, bij voorkeur bij een temperatuur lager tussen 0 en 5°C. Zoals bekend coaguleren de caseïne-eiwitten niet bij temperaturen lager dan 5°C. Wanneer de pH echter bij een temperatuur van 50°C wordt verlaagd, vlokken de caseïne-eiwitten bij het passeren van het isoelektrische punt (pH ongeveer 4,5) momentaan uit en deze uitvlokking blijkt bij de pH van ultrafiltratie (ongeveer 3) niet aanstonds reversibel.
Toevoeging van koud water leverde dan een lijm op. Uit caseïne kan met behulp van formaldehyde caseïneplastic of kunsthoorn gemaakt worden. Caseïne wordt gewonnen door afgeroomde melk met water te verdunnen en er vervolgens azijnzuur aan toe te voegen zodat de caseïne neerslaat. Caseïne kan op industriële schaal uit ondermelk gewonnen worden door de melk te verwarmen en aan te zuren met zwavelzuur.
Toepassingen van Caseïne
Naast toepassing in de voedingsindustrie heeft kaasstof ook andere toepassingen. In de schilderkunst wordt het toegepast om kleurstof te binden. Door caseïne in kalkwater of natronloog op te lossen kunnen kleuren geprepareerd worden die tegen weersinvloeden bestand zijn en bijgevolg bijzonder geschikt om wandschilderingen te maken op droge pleisterkalk. Kaasstof werd reeds lang gebruikt als lijmstof (kwarklijm), waartoe kalk als toeslag werd gebruikt. Omstreeks 1912 begon men in Zwitserland met de industriële productie van caseïnelijm.
Melkeiwitten zijn van groot belang. Zij zijn vrijwel onmisbaar bij het samenstellen van een groot aantal voedingsmiddelen, zoals zoetwaren, bakkerijprodukten en vleeswaren, zulks in het bijzonder vanwege hun goede smaak, hoge voedingswaarde alsmede hun gunstige bijdrage aan de textuur van bedoelde voedingsmiddelen.
Caseïne wordt ook veel gebruikt in eiwitsupplementen. Het heeft antikatabole eigenschappen, wat betekent dat het spierafbraak kan voorkomen, vooral tijdens de nacht. Dit komt door de langzame absorptiesnelheid van caseïne, die ervoor zorgt dat aminozuren geleidelijk aan het lichaam worden afgegeven.
Verschillende Vormen van Caseïne
- Calciumcaseïnaat: Meestal een geconcentreerd product. Caseïne is hier gedenatureerd en heeft zijn structuur (de micellen) verloren. De opname verloopt daardoor minder vlot.
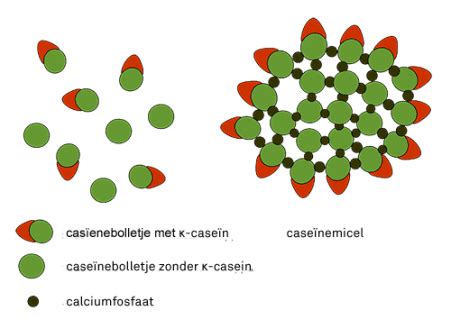
- Micellaire caseïne: Een soort van caseïne-isolaat. Het eiwit wordt bewaard waardoor de aminozuren zich langzaam kunnen verspreiden. Deze stof zit ook in de eiwitten van volle melk. Micellaire caseïne is de puurste vorm waarin caseïne-eiwit voorkomt en wordt vaak gekozen door sporters.
Caseïne en Lactose
Het is belangrijk om caseïne te onderscheiden van lactose. Caseïne is een eiwit, terwijl lactose een suiker is die aanwezig is in melk. Lactose-intolerantie is gerelateerd aan de afwezigheid of onvoldoende hoeveelheid van het enzym lactase, dat verantwoordelijk is voor de vertering van lactose. Lactosevrije melk bevat nog steeds caseïne, aangezien dit een natuurlijk eiwit is dat onafhankelijk van lactose aanwezig is.
Caseïne-intolerantie en Allergie
Caseïne-intolerantie is de ernstigste vorm van koemelkeiwitallergie. Voedselallergieën voor melkeiwitten, waaronder caseïne, komen het vaakst voor bij baby's en kinderen jonger dan drie jaar. Een caseïne-allergie treedt op wanneer het immuunsysteem het caseïne-eiwit als "schadelijk" herkent, wat kan leiden tot symptomen zoals buikpijn, een opgeblazen gevoel, jeukende huid en in extreme gevallen anafylactische shock. Er is geen effectieve behandeling met medicijnen; zuivelproducten moeten uit het dieet worden geschrapt. Het is raadzaam om een diëtist te raadplegen voor persoonlijk voedingsadvies.

Isolatie van caseïne-eiwit uit melk | Caseïne-eiwitisolatie | Hoe isoleer je caseïne-eiwit

tags: #denaturatie #van #caseine