Eiwitten zijn fundamentele bouwstenen van het leven, en hun structuur en functie zijn nauw verbonden met hun molecuulgewicht. In de context van melk, een rijke bron van voedingsstoffen, spelen caseïne-eiwitten een cruciale rol. Dit artikel duikt dieper in het molecuulgewicht van caseïne-eiwitten, hun eigenschappen en toepassingen.
Wat is Caseïne?
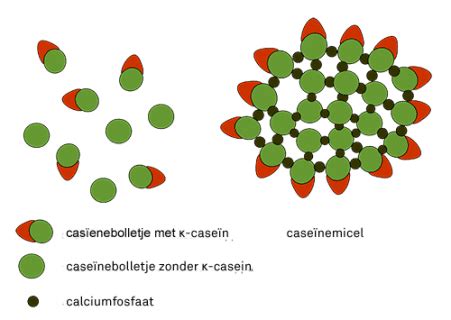
Caseïne is een dierlijk eiwit dat in melk voorkomt en veruit het belangrijkste melkeiwit is. In koemelk bestaat ongeveer 80% van alle eiwitten uit caseïne, terwijl dit aandeel in moedermelk lager ligt, variërend tussen 20% en 60% afhankelijk van de fase van de borstvoeding. Chemisch gezien is caseïne een fosfoproteïne, wat betekent dat er fosfaatgroepen aan zijn gekoppeld. Deze fosfaatgroepen spelen een belangrijke rol doordat ze calcium binden. In melk aggregeren caseïne-eiwitten tot microscopisch kleine bolletjes, de zogenaamde caseïnemicellen.
Molecuulgewicht en Eigenschappen van Caseïne
De specifieke eiwitten in melk, waaronder caseïnen, onderscheiden zich door hun molecuulgewicht, dat varieert van 14.000 dalton tot 100.000 dalton. Een kenmerkende eigenschap van caseïne is dat het in de maag klontert wanneer het in aanraking komt met maagzuur. Dit klonteren vertraagt de maaglediging, waardoor de aminozuren geleidelijk in de darm vrijkomen. Daardoor stijgt het aminozuurgehalte in het bloed langzamer en langer dan bij wei-eiwit, dat juist snel wordt opgenomen.
Caseïne bestaat uit verschillende subtypes, waaronder alfaS1-caseïne, alfaS2-caseïne, bèta-caseïne en kappa-caseïne. Vooral bèta-caseïne heeft de laatste jaren veel aandacht gekregen. Bèta-caseïne maakt ongeveer 30% uit van alle caseïne in koemelk en komt voor in twee veelbesproken varianten: A1 en A2. Het verschil tussen deze varianten zit in één enkel aminozuur op positie 67 van de keten van 229 aminozuren. Bij A2-bèta-caseïne is dit proline, terwijl het histidine is bij A1-bèta-caseïne. Inheemse runderrassen (Bos indicus) produceren van nature vooral A2-melk, terwijl veel Europese rassen (Bos taurus) de A1-variant dragen.
Analyse en Hydrolyse van Eiwitten
Bij de analyse van het eiwitgehalte wordt doorgaans eerst het stikstofgehalte bepaald, dat vervolgens met een N-factor wordt omgerekend naar het ruw eiwitgehalte. De methode van Dumas, ook bekend als methode voor de bepaling van stikstof door verbranding, bestaat uit een volledige verbranding van de organische matrix onder zuurstof. De geproduceerde gassen worden gereduceerd met koper, gedroogd en vervolgens wordt de kooldioxide afgevangen. Het stikstof wordt dan gekwantificeerd met een universele detector. Het totale eiwittengehalte wordt verkregen door het in percentage droog productgewicht uitgedrukte stikstofgehalte te vermenigvuldigen met een factor 6,25.
Met technieken zoals Gel Permeatie Chromatografie (GPC) is het mogelijk om eiwitten op basis van hun molecuulgewicht te scheiden. Deze techniek leent zich ook voor het vaststellen of eiwitten gehydrolyseerd zijn, hetzij bewust door toevoeging van enzymen, hetzij door ongewilde bacteriologische afbraak. Hydrolyse van eiwitten leidt tot de vorming van peptiden, die een kleiner molecuulgewicht hebben dan het niet-gehydrolyseerde eiwit. Naast melkeiwitten kunnen ook andere eiwitmengsels gekarakteriseerd worden, zoals bijvoorbeeld vis-eiwit hydrolysaat.
Vooral bij plantaardige eiwitten, zoals tarwe-eiwit, kan hydrolyse de oplosbaarheid en verteerbaarheid verbeteren. Tarwe-eiwitten met een gemiddelde molecuulmassa tussen 7 en 1000 kDa kunnen door middel van hydrolyse verwerkt worden. De hydrolysegraad ligt typisch tussen 1 en 4, vaak tussen 1,5 en 2,5. Gehydrolyseerd tarwe-eiwit met een oplosbaarheid van ten minste 55% bij pH 7 (NSI) wordt als voordelig beschouwd.
Toepassingen van Caseïne
Naast de voedingswaarde heeft caseïne ook diverse praktische toepassingen. Wanneer melk wordt aangezuurd of gestremd met stremsel, vormt caseïne de vaste massa die de basis is van kaas. Daarbuiten wordt caseïne al eeuwenlang gebruikt als bindmiddel in verf en lijm, en als grondstof voor bepaalde kunststoffen.

Voedingsindustrie
In de voedingsindustrie is caseïne een veelgebruikt ingrediënt, vooral bij de productie van zuivelproducten zoals kaas en yoghurt. Het zorgt voor de kenmerkende romige textuur en fungeert als een bron van hoogwaardige eiwitten. Bij het maken van kaas is caseïne essentieel, omdat het stolt om wrongel te vormen. Deze wrongel wordt vervolgens geperst en gerijpt om verschillende soorten kaas te produceren. Caseïne wordt ook gebruikt in bakkerijproducten om de voedingswaarde en textuur te verbeteren, en draagt bij aan de zachtheid en het vochtbehoud.
Voedingssupplementen
Caseïne-eiwitsupplementen zijn populair onder atleten en fitnessenthousiastelingen vanwege hun langzame vertering, wat zorgt voor een langdurige afgifte van aminozuren ter ondersteuning van spierherstel en -groei. Het heeft uitstekende hechtingseigenschappen en wordt vaak gebruikt in formules op waterbasis.
Industriële en Farmaceutische Toepassingen
In industriële toepassingen maken de hechtende eigenschappen van caseïne het waardevol in de formulering van verf, coatings en kleefstoffen. Het wordt al lang gebruikt als lijmstof, waarbij kalk als toeslag wordt toegevoegd. Omstreeks 1912 begon men met de industriële productie van caseïnelijm door de kwarklijm te drogen en tot poeder te verwerken. Uit caseïne kan met behulp van formaldehyde caseïneplastic of kunsthoorn worden gemaakt. In de farmaceutische sector wordt caseïne gebruikt als hulpstof, waar het fungeert als bindmiddel, desintegratiemiddel of vulstof in tablet- en capsuleformules. Het wordt ook gebruikt bij de productie van micro-inkapseling van geneesmiddelen.
Caseïne in Moedermelk
Moedermelk is de primaire bron van voeding voor pasgeborenen en speelt een cruciale rol in hun immuunsysteem. De eiwitten in moedermelk zijn divers, waaronder caseïne. β-Caseïne is de voornaamste caseïne in moedermelk en kan calciumionen binden, wat bijdraagt aan de hoeveelheid calcium in de melk. Ook κ-caseïne komt voor in moedermelk en heeft aangetoond de bacterie Helicobacter pylori tegen te werken.
Naast caseïne bevat moedermelk ook andere belangrijke eiwitten zoals α-lactalbumine, dat calcium- en zinkionen kan binden en mogelijk een positieve invloed heeft op de opname van mineralen, evenals een antimicrobiële functie. De meest voorkomende immunoglobuline in moedermelk is IgA, die antilichamen bevat tegen diverse bacteriën. Lactoferrine, een ander belangrijk eiwit, bindt ijzer en stimuleert de ijzeropname in de darmen van de zuigeling, en heeft tevens antimicrobiële werking.

Wat voeding doet met je brein: een nieuwe visie op mentale gezondheid
De eiwitten in moedermelk dragen bij aan de bescherming tegen infecties en de ontwikkeling van de darmflora bij zuigelingen. De samenstelling van moedermelk, inclusief het aandeel caseïne, kan variëren afhankelijk van factoren zoals de voedingsinname van de moeder en het tijdstip van de dag.
tags: #molecculgewicht #caseine #eiwitten